हाइड्रोजन आबंध किसे कहते हैं कितने प्रकार का होता है, गुण, उपयोग, उदाहरण, हाइड्रोजन बंध
हाइड्रोजन आबंध किसे कहते हैं कितने प्रकार का होता है, गुण, उपयोग, उदाहरण, हाइड्रोजन बंध
हाइड्रोजन आबंध
वह आकर्षण बल जो किसी एक अणु के हाइड्रोजन परमाणु को किसी दूसरे समान या असमान अणु के विद्युत ऋणात्मक परमाणु से बांधता है। उस आकर्षण बल को हाइड्रोजन आबंध (hydrogen bond in Hindi) कहते हैं।
अगर दूसरे शब्दों में कहें, तो जब कोई हाइड्रोजन परमाणु किसी प्रबल ऋण विद्युती परमाणु से जुड़ा होता है। तो वह किसी अन्य ऋण विद्युती परमाणु के साथ एक अपेक्षाकृत क्षीण बंध बना लेता है इस बंध को हाइड्रोजन आबंध कहते हैं।
हाइड्रोजन आबंध को कटी लाइनों (———- dotted lines ) द्वारा प्रदर्शित किया जाता है। तथा (—) द्वारा सहसंयोजक बंध को दर्शाते हैं। चित्र द्वारा स्पष्ट किया गया है।
हाइड्रोजन आबंध के उदाहरण
1. हाइड्रोजन फ्लुओराइड HF में अणु एक दूसरे से हाइड्रोजन बंध द्वारा जुड़े रहते हैं। जिन्हें नीचे चित्र द्वारा प्रस्तुत किया गया है।
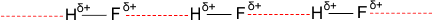
H—F में हाइड्रोजन परमाणु फ्लुओराइड से सहसंयोजी बंध द्वारा जुड़ा रहता है। तथा यह दूसरे H—F अणु के F से एक अतिरिक्त हाइड्रोजन आबंध बना लेता है।
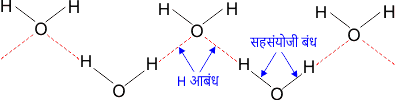
2. जल H2O के अणुओं में हाइड्रोजन आबंध को चित्र द्वारा प्रदर्शित किया गया है। ऑक्सीजन परमाणु से सहसंयोजक आबंध द्वारा जुड़ा हाइड्रोजन परमाणु, दूसरे H2O अणु के ऑक्सीजन परमाणु से हाइड्रोजन आबंध बना लेता है।
हाइड्रोजन आबंध के प्रकार
हाइड्रोजन आबंध दो प्रकार के होते हैं।
1. अंतरा अणुक हाइड्रोजन आबंध
2. अंतर अणुक हाइड्रोजन आबंध
1. अंतरा अणुक हाइड्रोजन आबंध
जब दो या अधिक अणुओं के मध्य हाइड्रोजन आबंध बनते हैं। तो उन्हें अंतरा अणुक हाइड्रोजन आबंध कहते हैं।
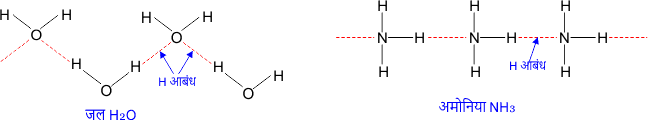
उदाहरण – जल H2O, अमोनिया NH3 आदि। इनकी संरचना को चित्र द्वारा दर्शाया गया है।
2. अंतर अणुक हाइड्रोजन आबंध
जब एक ही अणु के भीतर हाइड्रोजन आबंध बनता है तो उन्हें अंतरण हाइड्रोजन आबंध कहते हैं।
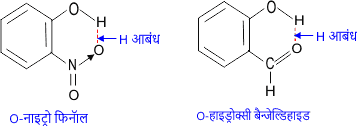
उदाहरण – ऑर्थो-नाइट्रो फिनॉल तथा ऑर्थो-हाइड्रोक्सी बैंजेल्डिहाइड में अंतर अणुक हाइड्रोजन आबंध होता है। चित्र में दर्शाया गया है।
Note – हाइड्रोजन आबंध सममित तथा असममित प्रकार के होते हैं।
वह हाइड्रोजन आबंध जिसमें हाइड्रोजन परमाणु दो परमाणु नाभिकों के बीच में स्थित होता है। तो उन्हें सममित हाइड्रोजन आबंध कहते हैं।
हाइड्रोजन बाइफ्लुओराइड F—H—–F– सममित हाइड्रोजन आबंध का उदाहरण है।
वह हाइड्रोजन आबंध जिसमें हाइड्रोजन परमाणु दो नाभिकों के मध्य नहीं होता है तो उन्हें असममित हाइड्रोजन आबंध कहते हैं। अधिकांश हाइड्रोजन आबंध असममित ही होते हैं। हाइड्रोजन फ्लुओराइड F—H—-F असममित हाइड्रोजन आबंध का एक उदाहरण है।