Bihar Board Class 9Th Science chapter 3 परमाणु एवं अणु (Atoms and Molecules) Solutions | Bseb class 9Th Chapter 3 परमाणु एवं अणु (Atoms and Molecules) Notes
Bihar Board Class 9Th Science chapter 3 परमाणु एवं अणु (Atoms and Molecules) Solutions | Bseb class 9Th Chapter 3 परमाणु एवं अणु (Atoms and Molecules) Notes
प्रश्न- अणु एवं परमाणु की परिभाषा लिखें ।
उत्तर— परमाणु – डाल्टन के परमाणु सिद्धांत के अनुसार, पदार्थ की अति सूक्ष्म एवं अविभाज्य कण परमाणु कहलाती है।
या,
तत्त्व का सूक्ष्मतम कण, जो रासायनिक अभिक्रियाओं में भाग ले सकते हैं, परमाणु कहलाते हैं ।
अणु – दो या दो से अधिक परमाणुओं से बना पदार्थ का सबसे छोटा कण जो स्वतंत्र रूप में रह सकता है, अणु कहलाता हैं
प्रश्न- रासायनिक संयोग के नियमों को लिखें।
उत्तर— द्रव्यमान संरक्षण का नियम – किसी भी रासायनिक अभिक्रिया में क्रियाशील पदार्थों के द्रव्यमान में न तो कमी आती है न ही इसमें वृद्धि होती है।
स्थिर अनुपात का नियम – किसी भी यौगिक के निर्माण में प्रयुक्त होने वाले तत्व एक निश्चित द्रव्यमानों के अनुपात में विद्यमान रहते हैं।
उदाहरण – जल में हाइड्रोजन व ऑक्सीजन के द्रव्यमानों का अनुपात हमेशा 1:8 रहता है।
प्रश्न- डाल्टनके परमाणु सिद्धांतों को लिखो।
उत्तर— डाल्टन के परमाणु सिद्धांत निम्न है—
(i) सभी पदार्थ अति सूक्ष्म एवं अविभाज्य कणों से मिलकर बने होते हैं, जिसे परमाणु कहते हैं।
(ii) किसी भी रासायनिक अभिक्रिया में परमाणु का न तो सृजन होता है और न ही इसका विनाश होता है।
(iii) एक ही तत्व के परमाणुओं के द्रव्यमान एवं गुण समान होते हैं।
(iv) अलग-अलग तत्वों के परमाणुओं के द्रव्यमान भिन्न होते हैं।
(v) रासायनिक संयोग में विभिन्न तत्त्वों के परमाणु सरल सांख्यिक अनुपात जैसे 1 : 2, 2 : 3, 1 : 3 आदि में संयोग करते हैं।
प्रश्न- आवोगादो स्थिरांक का मान लिखो।
उत्तर— 6.022 x 1023
प्रश्न- मोलर द्रव्यमान को परिभाषित करें ।
उत्तर— पदार्थ के एक मोल अणुओं का द्रव्यमान उसका मोलर द्रव्यमान कहलाता है।
प्रश्न- हाइड्रोजन एवं ऑक्सीजन द्रव्यमान के अनुसार 1 : 8 के अनुपात में संयोग करके जल निर्मित करते हैं । 3g हाइड्रोजन गैस के साथ पूर्ण रूप से संयोग करने के लिए कितने ऑक्सीजन गैस के द्रव्यमान की आवश्यकता होगी ?
उत्तर— 18 हाइड्रोजन के लिए 8g ऑक्सीजन चाहिए । अतः 3g हाइड्रोजन के लिए 3 x 8 = 24g ऑक्सीजन चाहिए ।
प्रश्न- डाल्टन के परमाणु सिद्धांत का कौन-सा अभिग्रहीत द्रव्यमान के संरक्षण के नियम का परिणाम है ?
उत्तर— परमाणु अविभाज्य सूक्ष्मतम कण होते हैं जो रासायनिक अभिक्रिया में न तो सृजित होते हैं और न ही उनका विनाश होता है ।
प्रश्न- परमाणु द्रव्यमान इकाई को परिभाषित कीजिए।
उत्तर— कार्बन-12 समस्थानिक के एक परमाणु द्रव्यमान के 1/12 वें भाग को मानक परमाणु द्रव्यमान इकाई कहते हैं।
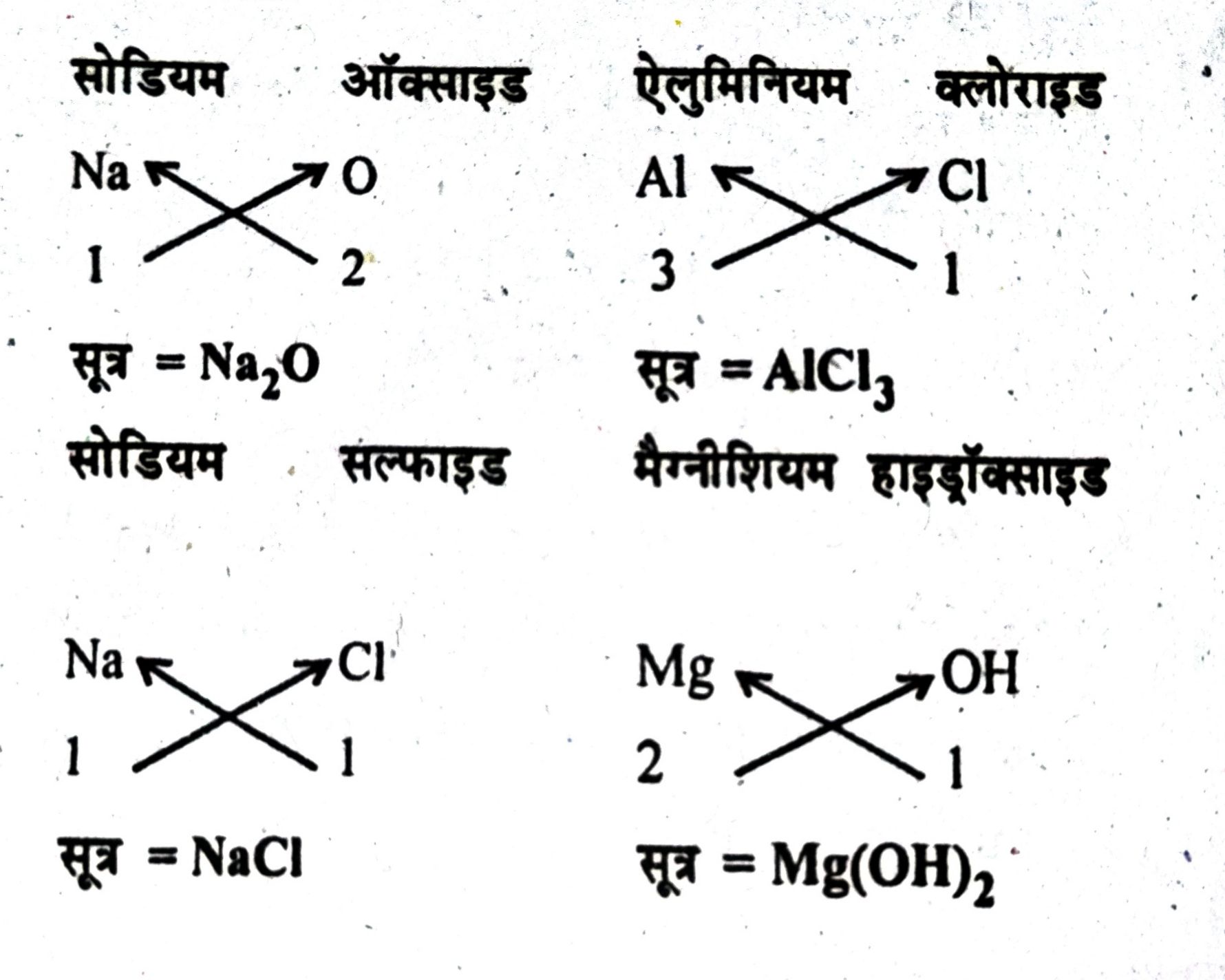
प्रश्न- निम्न के सूत्र लिखिए—
(i) सोडियम ऑक्साइड (II) ऐलुमिनियम क्लोराइड (III) सोडियम सल्फाइड (iv) मैगनीशियम हाइड्रॉक्साइड
उत्तर—
प्रश्न- निम्नलिखित सूत्रों द्वारा प्रदर्शित यौगिकों के नाम लिखिए— (i) Al2 (SO4)3 (ii) CaCl2 (III) K2SO4 (iv) KNO3 (v) CaCO3
उत्तर— (i) Al2 (SO4 )3 – ऐलुमिनियम सल्फेट
(ii) CaCl2 – कॉपर क्लोराइड
(iii) K2SO4 – पोटैशियम सल्फेट
(iv) KNO3 – पोटैशियम नाइट्रेट
(v) CaCO3 – कैल्सियम कार्बोनेट
प्रश्न- रासायनिक सूत्र का क्या तात्पर्य है ?
उत्तर— किसी यौगिक का रासायनिक सूत्र उसके संघटक का प्रतीकात्मक निरूपण होता है ।
प्रश्न- निम्न में कितने परमाणु, विद्यमान हैं ?
(i) H2S अणु एवं (ii) PO43- आयन ?
उत्तर— (i) H2S में तीन परमाणु हैं ।
(ii) PO43- आयन में पाँच परमाणु हैं ।
प्रश्न- निम्न यौगिकों के सूत्र इकाई द्रव्यमान का परिकलन कीजिए—
ZnO, Na2O एवं K2CO3
दिया गया है :
Zn का परमाणु द्रव्यमान = 65 u
Na का परमाणु द्रव्यमान = 23 u
K का परमाणु द्रव्यमान = 39 u
C का परमाणु द्रव्यमान = 12 u
O का परमाणु द्रव्यमान = 16 u
उत्तर— ZnO = Zn + O
= 65 + 16 = 91 u
Na2O = 2Na + 0
= 2 x 23 + 16 = 46 + 16 = 62 u
K2CO3 = 2K + C + 3 0
= 2 x 39 + 12 + 3 x 16 = 78 + 12 + 48 = 138 u
प्रश्न- यदि कार्बन परमाणुओं के एक मोल का द्रव्यमान 12g है तो कार्बन के एक परमाणु का द्रव्यमान क्या होगा ?
उत्तर— 1 मोल में परमाणुओं की संख्या = 6.022 x 1023
6.022 x 1023 परमाणुओं का द्रव्यमान = 12 g
1 परमाणु का द्रव्यमान = 12/6.022 x 1023 = 12000 x 10– 23 = 1.99 x 10– 23 g.
प्रश्न- 0.24g ऑक्सीजन एवं बोरॉन युक्त यौगिक के नमूने में विश्लेषण द्वारा यह पाया गया कि उसमें 0.096g बोरॉन एवं 0.144g ऑक्सीजन है । उस यौगिक के प्रतिशत संघटन का भारात्मक रूप में परिकलन कीजिए ।
उत्तर— बोरॉन प्रतिशतता = बोरॉन का द्रव्यमान / यौगिक का द्रव्यमान x 100
= 0.096 / 0.24 x 100 = 40%
ऑक्सीजन प्रतिशतता = ऑक्सीजन का द्रव्यमान / यौगिक का द्रव्यमान x 100
= 0.144 / 0.24 x 100 = 60%
प्रश्न- 3.0g कार्बन 8.00g ऑक्सीजन में जलकर 11.00g कार्बन डाइऑक्साइड निर्मित करता है। जब 3.00g कार्बन को 50.00g ऑक्सीज़न में जलाएँगे तो कितने ग्राम कार्बन डाइऑक्साइड का निर्माण होगा ? आपका उत्तर रासायनिक संयोजन के किस नियम पर आधारित होगा ?
उत्तर— स्थिर अनुपातके नियम से 3g कार्बन मात्र 8g ऑक्सीजन के साथ ही अभिक्रिया करेगी क्योंकि CO2 में C: O= 3 : 8 के द्रव्यमान का अनुपात 3 : 8 है ।
कार्बन ऑक्सीजन कार्बनडाइऑक्साइड
3g + 50g =(3 + 8)g = 11 g
बाकी का 42g ऑक्सीजन बचा रह जाएगा ।
प्रश्न- निम्न का द्रव्यमान क्या होगा :
(a) 0.2 मोल ऑक्सीजन परमाणु ? (b) 0.5 मोल जल अणु ?
उत्तर— (a) ⇒ m = M x n ⇒ m = 16 × 0.2 = 3.2g
(b) द्रव्यमान = मोलर द्रव्यमान x मोल संख्या
= m = 18 × 0.5 = 9 g
हमसे जुड़ें, हमें फॉलो करे ..
- Telegram ग्रुप ज्वाइन करे – Click Here
- Facebook पर फॉलो करे – Click Here
- Facebook ग्रुप ज्वाइन करे – Click Here
- Google News ज्वाइन करे – Click Here