Bihar Board Class 9Th Science chapter 4 परमाणु की संरचना (Structure of Atom) Solutions | Bseb class 9Th Chapter 4 परमाणु की संरचना (Structure of Atom) Notes
Bihar Board Class 9Th Science chapter 4 परमाणु की संरचना (Structure of Atom) Solutions | Bseb class 9Th Chapter 4 परमाणु की संरचना (Structure of Atom) Notes
प्रश्न- परमाणु के तीन अव परमाणुक कणों के नाम लिखो ?
उत्तर— इलेक्ट्रॉन, प्रोटॉन, न्यूट्रॉन
प्रश्न- कैनाल किरणें क्या हैं ?
उत्तर— केनाल किरण– ई. गोल्डस्टीन के अनुसार यदि विसर्ग नली के कैथोड में पतली छेद कर दी जाए और (0.01 mm of Hg) दाब और 10,000 V पर विद्युत धारा प्रवाहित की जाए तो कुछ विशेष प्रकार की किरणे ऐनोड से कैथोड की ओर गमन करने लगती है जिन्हें केनाल किरणें या ऐनोड किरण कहा जाता है।
प्रश्न- रदरफोर्ड के परमाणु मॉडल के अनुसार, परमाणु के नाभिक में कौन-सा अवपरमाणुक कण विद्यमान है ?
उत्तर— प्रोटॉन (धनावेशित) होता है ।
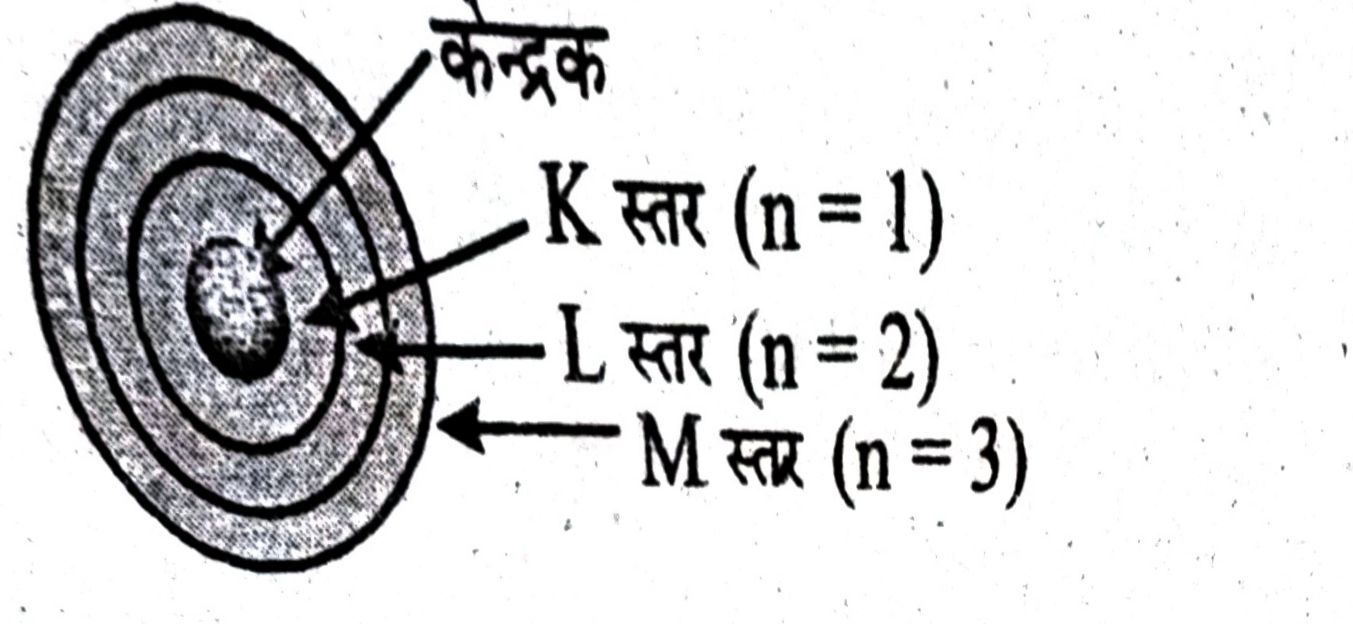
प्रश्न- तीन कक्षाओं वाले बोर के परमाणु मॉडल का चित्र बनाइए।
उत्तर—
प्रश्न- क्या अल्फा कणों का प्रकीर्णन प्रयोग सोने के अतिरिक्त दूसरी धातु की पन्नी से संभव होगा ?
उत्तर— यदि सोने के अलावा किसी अन्य धातु का उपयोग किया जाए, तो हो सकता है कि वे धातु α – कणों के साथ अभिक्रिया कर लें, अथवा धातु के कम आघातवर्ध्य होने के कारण α- कण उसकी मोटी पन्नी के परमाणुओं को भेद न पाएँ । अतः सोने के अलावा दूसरी धातु का प्रयोग संभव हीं है ।
प्रश्न- कार्बन और सोडियम के परमाणुओं के लिए इलेक्ट्रॉन-वितरण लिखिए।
उत्तर—
| तत्व का नाम | परमाणु क्रमांक | इलेक्ट्रॉनिक विन्यास |
| 6 | K L M | |
|
कार्बन
सोड़ियम
|
11 |
2 4
2 8 1
|
प्रश्न- अगर किसी परमाणु का K और L कोश भरा है, तो उस परमाणु में इलेक्ट्रॉनों की संख्या क्या होगी ?
उत्तर— (2 + 8) = 10 इलेक्ट्रॉन ।
प्रश्न- क्लोरीन, सल्फर और मैग्नीशियम की परमाणु संख्या से आप इनकी संयोजकता कैसे प्राप्त करेंगे ?
उत्तर— तत्त्व की इलेक्ट्रॉनिक विन्यास से संयोजकता इलेक्ट्रोन का पता चलता है यदि संंयोजकता इलेक्ट्रॉन 1, 2, 3 या 4 हो तो संयोजकता भी उतना ही रहता है । संयोजी इलेक्ट्रॉन 5 या उससे ज्यादा रहे तो संयोजकता निकालने के लिए इसे 8 से घटा लिया जाता है ।
| तत्व का नाम | परमाणु संख्या | इलेक्ट्रॉनिक विन्यास | संयोजी इलेक्ट्रॉन | संयोजकता |
| K L M | ||||
| क्लोरीन | 17 | 2 8 7 | 7 | 8 – 7= 1 |
| सल्फर | 16 | 2 8 6 | 6 | 8 – 6 = 2 |
| मैग्नीशियम | 12 | 2 8 2 | 2 | 2 |
प्रश्न- समस्थानिक और समभारिक के किसी एक युग्म का इलेक्ट्रॉनिक विन्यास लिखिए।
उत्तर— (i) समभारिक – 40/20 Ca और 40/18 Ar
Ca का इलेक्ट्रॉनिक विन्यास = 2, 8, 8, 2
Ar का इलेक्ट्रॉनिक विन्यास = 2, 8, 8
(ii) समस्थानिक–12/6 C और 4/6 C
C इलेक्ट्रॉनिक विन्यास = 2,4
प्रश्न- इलेक्ट्रॉन, प्रोटॉन और न्यूट्रॉन के गुणों की तुलना कीजिए।
उत्तर— 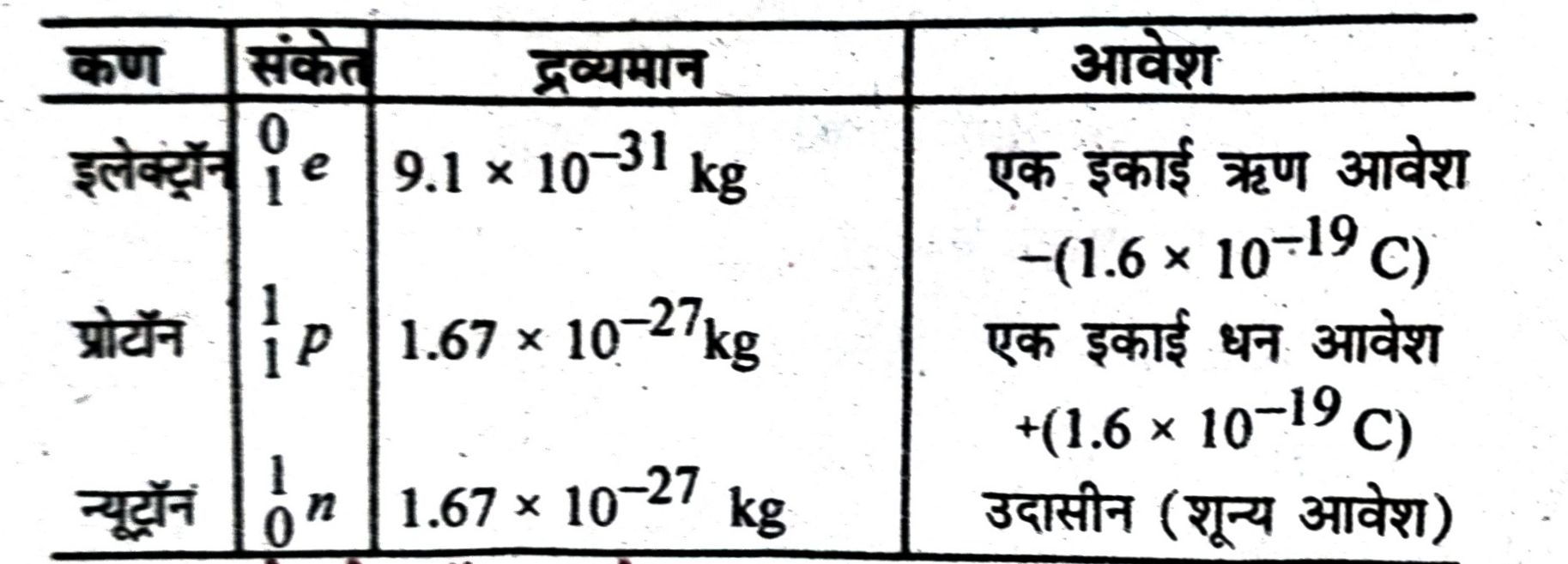

प्रश्न- जे. जे. टॉमसन के परमाणु मॉडल की क्या सीमाएँ है ?
उत्तर— (i) जे. जे. टॉमसन द्वारा प्रस्तावित परमाणु मॉडल अन्य वैज्ञानिकों जैसे रदरफोर्ड द्वारा गलत साबित कर दिये गये ।
(ii) यह मॉडल परमाणु के स्थिरता (stability) के कारण की पुष्टि नहीं करता है।
(iii) अन्य वैज्ञानिकों द्वारा परमाणुओं पर किये गये प्रयोगों के परिणाम इस मॉडल द्वारा नहीं समझाया जा सका ।
प्रश्न- रदरफोर्ड के परमाणु मॉडल की क्या सीमाएँ है ?
उत्तर— (i) रदरफोर्ड मॉडल की कक्षाओं में उपस्थिति इलेक्ट्रोनों की संख्या निश्चित नहीं की गई थी ।
(ii) रदरफोर्ड के मॉडल के अनुसार प्रोटोन परमाणु के नाभिक में स्थित होता है जबकि इलेक्ट्रॉन इसके चारो ओर चक्कर लगाते हैं। अन्य वैज्ञानिकों के राय से इलेक्ट्रॉन यदि चक्कर लगाती है तो उसके पास कुछ न कुछ त्वरण अवश्य होगा जिसके फलस्वरूप यह ऊर्जा का विकिरण करेगी और किसी समय नाभिक से जा टकराएगी। अतः इससे कोई भी परमाणु नियमित (stable) नहीं रह सकता ।
प्रश्न- बारे के परमाणु मॉडल की व्याख्या करें ।
उत्तर— बोर परमाण्विक मॉडल की मूल अवधारणाएँ निम्न हैं—
(i) किसी भी परमाणु में इलेक्ट्रॉन नाभिक के चारो तरफ एक निश्चित चक्रीय पथ पर घूमते हैं। ये चक्रीय पथ इलेक्ट्रॉन कक्ष या Orbit कहलाते हैं।
(ii) इस कक्ष में घूमते हुए इलेक्ट्रॉन ऊर्जा का विकिरण है।
(iii) इलेक्ट्रॉन कक्ष या ऊर्जा स्तरों को 1, 2, 3, 4… या K, L, M,N द्वारा सूचित किया जाता है।
(iv) एक कक्ष से दूसरे कक्ष में जाने पर इलेक्ट्रॉन ऊर्जा मुक्त करती है।
प्रश्न- उदाहरण के साथ व्याख्या कीजिए परमाणु संख्या, द्रव्यमान संख्या समस्थानिक और समभारिक समस्थानिकों के कोई दो उपयोग लिखिए।
उत्तर— (i) किसी तत्व के एक परमाणु के नाभिक में मौजूद प्रोटॉनों की संख्या को उसकी परमाणु संख्या कहते हैं। इसे Z से सूचित करते हैं।
कार्बन के लिए Z = 6 क्योंकि कार्बन परमाणु के नाभिक में 6 प्रोटॉन होते हैं।
(ii) किसी तत्व के एक परमाणु के नाभिक में उपस्थित प्रोटॉनों और न्यूट्रॉनों की कुल संख्या उसकी द्रव्यमान संख्या कहलाती है। उदाहरण के लिए, कार्बन की द्रव्यमान संख्या 12 है क्योंकि उसमें 6 प्रोटॉन और 6 न्यूट्रॉन होते हैं (6 + 6 = 12)I
(iii) किसी तत्व के ऐसे परमाणु जिनकी परमाणु संख्या समान हो परन्तु द्रव्यमान संख्या भिन्न-भिन्न हो, उस तत्व के समस्थानिक कहलाते हैं ।
(i) हाइड्रोजन के तीन समस्थानिक होते हैं—
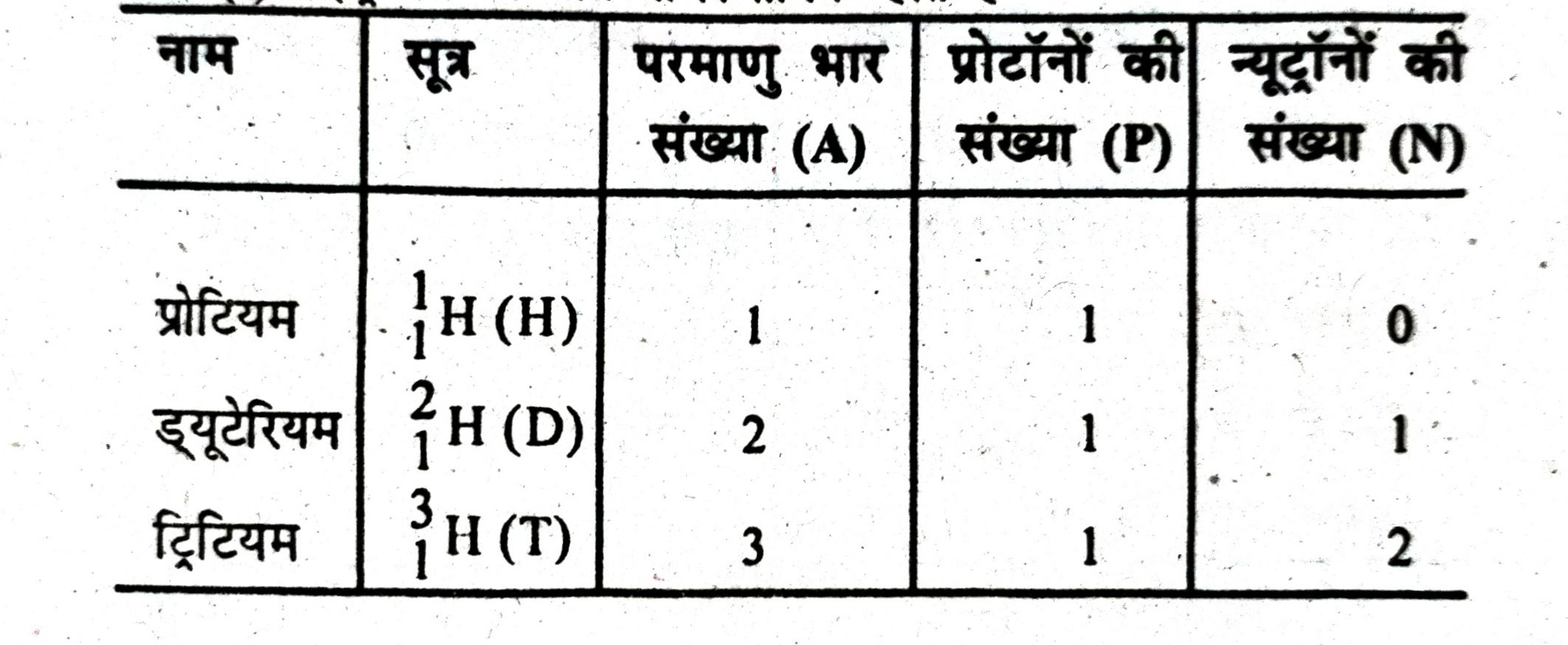
(iii) तत्वों के ऐसे परमाणु जिनकी द्रव्यमान संख्या तो समान हो परंतु परमाणु संख्या भिन्न हो, उन तत्वों के समभारिक परमाणु कहलाते हैं । उदाहरण
| तत्व का नाम | द्रव्यमान संख्या |
परमाणु संख्या
|
| कैल्सियम | 40 | 20 |
| आर्गन | 40 | 18 |
समस्थानिकों के कुछ उपयोग निम्नलिखित हैं—
(i) यूरेनियम का एक समस्थानिक परमाणु रिएक्टर में ईंधन के रूप में उपयोग किया जाता है।
(ii) कोबाल्ट का एक समस्थानिक कैंसर के इलाज में प्रयुक्त होता है।
(iii) आयोडीन का एक समस्थानिक घेंघा रोग के इलाज में प्रयुक्त होता है।
हमसे जुड़ें, हमें फॉलो करे ..
- Telegram ग्रुप ज्वाइन करे – Click Here
- Facebook पर फॉलो करे – Click Here
- Facebook ग्रुप ज्वाइन करे – Click Here
- Google News ज्वाइन करे – Click Here