धातुकर्म (Metallurgy)
धातुकर्म (Metallurgy)
धातुकर्म (Metallurgy)
अयस्कों से शुद्ध धातु प्राप्त करने की प्रक्रिया को धातुओं का निष्कर्षण कहते हैं। भू-पर्पटी (earth’s crust) में कुछ धातुएँ मुक्त अवस्था (free state) में पाई जाती हैं जबकि कुछ संयुक्त अवस्था में यौगिकों के रूप में पाई जाती हैं। एक तत्व के संयुक्त अवस्था से निष्कर्षण तथा पृथक्करण में रसायन के कई सिद्धान्त निहित होते हैं। फिर भी धातुओं के सभी निष्कर्षण प्रक्रमों के कुछ सामान्य सिद्धान्त समान है।
धातुकर्म (Metallurgy)
अयस्कों से धातु पृथक्करण में प्रयुक्त होने वाली सम्पूर्ण वैज्ञानिक व प्रौद्योगिक प्रक्रिया धातुकर्म कहलाती है। यह प्रक्रिया तीन प्रकार की हो सकती है
(i) हाइड्रोमेटेलर्जी (Hydrometallurgy) अर्थात् जलीय माध्यम में निष्कर्षण।
(ii) पायरोमेटेलर्जी (Pyrometallurgy) अर्थात् ऊष्मा के उपयोग द्वारा निष्कर्षण।
(iii) इलेक्ट्रोमेटेलर्जी ( Electrometallurgy) अर्थात् विद्युत के उपयोग द्वारा निष्कर्षण ।
धातुकर्म के प्रयोग में आने वाले पारिभाषिक शब्द (Terms Used in Metallurgy)
धातुकर्म के प्रयोग में आने वाले कुछ परिभाषिक शब्द इस प्रकार हैं
खनिज (Minerals)
भू-पर्पटी में प्राकृतिक रूप से पाए जाने वाले रासायनिक पदार्थ जो कि खनन द्वारा प्राप्त किए जा सकते हों, खनिज कहलाते हैं। उदाहरण बॉक्साइट और कार्नेलाइट।
◆ ऑक्सीजन भू-पर्पटी में सबसे अधिक प्रचुरता से पाया जाने वाला अधातु तत्व है जबकि ऐलमिनियम भू-पर्पटी में सबसे अधिक प्रचुरता से पाया जाने वाला धातु तत्व है।
◆ मानव शरीर में सर्वाधिक प्रचुरता में पाया जाने वाला तत्व ऑक्सीजन है।
अयस्क (Ore)
खनिज जिनसे धातु का निष्कर्षण विभिन्न पदों द्वारा लाभदायक रूप से किया जाता है, अयस्क कहलाते हैं। सभी खनिज अयस्क नहीं है लेकिन सभी अयस्क खनिज हैं। उदाहरण आयरन पायराइट आयरन का खनिज है लेकिन इसे अयस्क के रूप में नहीं समझा जा सकता है, क्योंकि इससे आयरन का निष्कर्षण बहुत महँगा है।

अयस्कों का सान्द्रण (Concentration of Ores)
अवांछित पदार्थों जैसे रेत, क्ले, आदि का अयस्कों से निष्कासन का प्रक्रम सान्द्रण (concentration), प्रसाधन (dressing) या सज्जीकरण (benefaction) कहलाता है। यह हाथों से चुनकर भी किया जा सकता है लेकिन अनेक दूसरी तकनीके भी प्रयोग की जा सकती हैं। इन तकनीकों का वर्णन इस प्रकार है
(i) द्रवीय धावन (Hydraulic Washing) यह विधि अयस्क तथा गैंग कणों के आपेक्षिक घनत्वों (relative density) के अन्तर पर निर्भर करती है। अतः यह गुरुत्वीय पृथक्करण (gravity separation) का एक प्रकार है। तेज धारा के साथ गैंग के हल्के कण बह जाते हैं और भारी अयस्क के कण शेष रह जाते हैं। उदाहरण आयरन के अयस्क (Fe2O3) और (Fe3O4) इस प्रक्रम द्वारा सान्द्रित किए जाते हैं।
(ii) चुम्बकीय पृथक्करण (Magnetic Separation) यह विधि अयस्क और गैंग के चुम्बकीय गुणों की भिन्नता पर आधारित है। उदाहरण क्रोमाइट अयस्क (FeO. Cr2O3) का सान्द्रण तथा दो अयस्कों वोल्फ्रेमाइट (टंगस्टन का चुम्बकीय अयस्क) का कैसिटेराइट (टिन का अचुम्बकीय अयस्क) से पृथक्करण इस प्रक्रम से किया जाता है।
(iii) फेन प्लवन विधि (Froth Floatation Method) यह विधि सल्फाइड अयस्कों को गैंग से मुक्त करने के लिए प्रयुक्त होती है। संग्राही चीड़ का तेल तथा फेन-स्थायीकारी (क्रिसॉल) को अयस्क के जल में निलम्बन में मिलाया जाता है। अयस्क के कण तेल से भीगकर फेन के साथ ऊपर आ जाते हैं जिन्हें मथकर निकाल लिया जाता है। जबकि गैंग के कण जल से भीग कर नीचे बैठ जाते हैं।
(iv) निक्षालन (Leaching) यदि अयस्क किसी उपयुक्त विलायक में विलेय हो तो प्रायः निक्षालन का उपयोग करते हैं। बॉक्साइट अयस्क का निक्षालन सान्द्र सोडियम हाइड्रॉक्साइड द्वारा तथा स्वर्ण और चाँदी का निक्षालन वायु की उपस्थिति में सोडियम अथवा पोटैशियम सायनाइड के तनु विलयन से किया जाता है।
सान्द्रित अयस्कों से अशोधित धातुओं का निष्कर्षण (Extraction of Crude Metal from Concentrated Ores)
सान्द्रित अयस्क से धातुओं का पृथक्करण निम्न दो मुख्य पदों में होता है
1. ऑक्साइड में परिवर्तन (Conversion to Oxide) यह निम्नलिखित दो प्रक्रियाओं द्वारा प्राप्त किया जाता है
(i) निस्तापन (Calcination) निस्तापन में गर्म करने की आवश्यकता होती है जिससे वाष्पशील पदार्थ निष्कासित हो जाते हैं और धातु ऑक्साइड शेष रह जाता है। धातु के कार्बोनेट, हाइड्रॉक्साइड तथा ऑक्साइड का निस्तापन करते हैं। ये पदार्थ छोटे अणुओं (जैसे CO2, H2O) के मुक्त होने के साथ अपने संगत ऑक्साइडों में अपघटित हो जाते हैं।
(ii) भर्जन (Roasting) यह केवल सल्फाइड अयस्कों के लिए हैं। इसमें अयस्क को धातु ऑक्साइड में परिवर्तित करने के लिए वायु की नियमित आपूर्ति में धातु के गलनांक से नीचे के तापमान पर एक भट्टी में गर्म किया जाता है। इस प्रक्रिया में सल्फर तथा आर्सेनिक आदि अशुद्धियाँ ऑक्सीकृत हो जाती हैं और वाष्पशील अशुद्धियों के रूप में बच निकलती हैं। संगत धातु ऑक्साइड शेष रह जाता है।
उदाहरण 
2. ऑक्साइड का धातु में अपचयन (Reduction of Oxide to Metal) ऑक्साइड का धातु में अपचयन निम्नलिखित प्रकार से किया जाता है
(i) प्रगलन (Smelting) यह कार्बन या इसके ऑक्साइडों द्वारा अपचयन है। सक्रियता श्रेणी के मध्य में स्थित धातुओं का अपचयन इस विधि से किया जाता है।
अयस्क को उसके द्रवणांक से ऊपर तापक्रम पर कोक और गालक के साथ मिलाकर गर्म करने की प्रक्रिया को प्रद्रावण या प्रगलन कहते हैं। लेड, आयरन, टिन, जिंक, आदि धातुओं के ऑक्साइड इस विधि से अपचयित किए जाते हैं। इस विधि का उपयोग पूरे मिश्रण को गलाने में तथा धातु ऑक्साइडों को धातु में अपचयित करने में किया जाता है।
उदाहरण 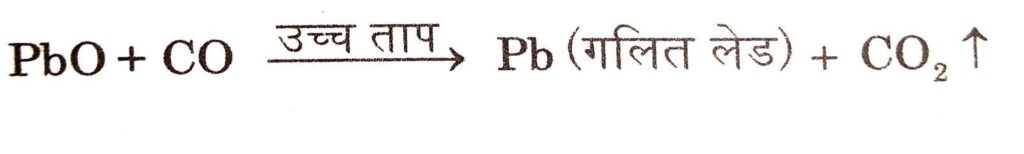
◆ गालक (Flux) यह प्रगलन के समय अयस्क में मिलाया जाने वाला अतिरिक्त (विशेष) पदार्थ है। अयस्क में उपस्थित अगलित पदार्थ गालक द्वारा गलित पदार्थ में परिवर्तित हो जाते हैं। उदाहरण आयरन के प्रगलन में लाइमस्टोन (CaCO3) गालक की तरह प्रयुक्त किया जाता है।
◆ गालक अम्लीय या क्षारीय हो सकते हैं। अम्लीय गालक जैसे SiO2 क्षारीय अशुद्धियाँ दूर करने में प्रयुक्त किया जाता है तथा क्षारीय गालक जैसे CaO, FeO आदि अम्लीय अशुद्धियाँ दूर करने में प्रयुक्त किया जाता है।
◆ धातुमल (Slag) हैं, इस पदार्थ को गालक के मिलाने पर अम्लीय या क्षारीय आधात्री द्रवणशील पदार्थ में परिवर्तित हो जाते धातुमल कहते हैं।
गालक + अम्लीय / क्षारीय अशुद्धियाँ → धातुमल
हल्का होने के कारण धातुमल गलित धातु की सतह पर तैरता है। उदाहरण आयरन के अयस्क में SiO2 अशुद्धियों के रूप में होता है, जो गालक CaO (1000°C पर CaCO3 से बनता है।) से संयोग करके घातुमल कैल्सियम सिलिकेट (CaSiO3) बनाता है।
SiO2 + CaO → CaSiO3
(ii) ऐलुमिनोथर्मिक प्रक्रम (Aluminothermic Process) क्रोमियम, मैंग्नीज, आदि धातुओं के ऑक्साइड ऐलुमिनियम द्वारा अपचयित किए जाते हैं।
उदाहरण Cr2O3 + 2Al → Al2O3 + 2Cr
(iii) स्वत: अपचयन (Auto-reduction) सक्रियता श्रेणी में नीचे आने वाली धातुएँ काफी कम सक्रिय होती है। इन धातुओं के ऑक्साइडों को केवल गर्म करने से ही धातु को प्राप्त किया जा सकता है। उदाहरण कॉपर, मर्करी, लैड का अपचयन इस विधि से किया जाता है।
(iv) विद्युत अपघटन विधि (Electrolytic Method) सक्रियता श्रेणी में सबसे ऊपर स्थित धातुएँ जैसे सोडियम, कैल्सियम, ऐलुमिनियम के लिए यह विधि प्रयोग की जाती है। इस विधि से इनके ऑक्साइड धातु में अपचयित हो जाते हैं। सोडियम क्लोराइड के अपघटन के फलस्वरूप सोडियम प्राप्त किया जाता है।
परिष्करण या शोधन (Refining)
किसी भी विधि द्वारा निष्कर्षण से प्राप्त धातुओं में सामान्य रूप से कुछ अशुद्धियाँ मिली रहती हैं। उचित दशाओं में अशुद्ध या कच्ची धातु से शुद्ध धातु के निष्कर्षण की विधि धातु का शोधन कहलाती है। यह धातु तत्व की प्रकृति तथा उसमें उपस्थित अशुद्धियों की प्रकृति पर निर्भर करती है। उच्च शुद्धता की धातु प्राप्त करने के लिए अनेक विधियाँ प्रयोग में लाई जाती हैं। ये इस प्रकार हैं
(i) आसवन (Distillation) Zn, Cd, Hg धातुओं का शोधन इस विधि से किया जाता है क्योंकि ये निम्न क्वथन धातु हैं।
(ii) द्रावगलन परिष्करण (Liquation) टिन, मर्करी, लेड जैसी धातुएँ इस विधि से शोधित की जाती हैं क्योंकि इनके गलनांक निम्न हैं।
(iii) विद्युत अपघटनी शोधन (Electrolytic Refining) कॉपर, सिल्वर, गोल्ड, ऐलुमिनियम और लेड धातु का शोधन इस विधि द्वारा किया जाता है। इस विधि में अशुद्ध धातु का ऐनोड तथा शुद्ध धातु का कैथोड बनाते हैं। धातु के लवण विलयन का उपयोग विद्युत अपघट्य के रूप में होता है।
(iv) मण्डल परिष्करण (Zone Refining) यह विधि इस सिद्धान्त पर आधारित है कि अशुद्धियों की विलेयता धातु की ठोस अवस्था की अपेक्षा गलित अवस्था में अधिक होती है। यह विधि अति उच्च शुद्धता अर्द्धचालकों तथा अन्य अतिशुद्ध धातुओं जैसे जर्मेनियम, सिलिकन, बोरॉन, गैलियम तथा इण्डियम को प्राप्त करने में उपयोगी है। वाले
(v) वाष्प प्रावस्था परिष्करण (Vapour Phase Refining) इस विधि में धातु को वाष्पशील यौगिक में परिवर्तित कर लिया जाता है। इसके पश्चात् इसे विघटित करके शुद्ध धातु प्राप्त कर लेते हैं।
उदाहरण
मॉण्ड प्रक्रिया (Mond Process )
यह निकैल के लिए प्रयुक्त किया जाता है।

वॉन – आर्केल विधि (van-Arkel Method)
यह जिर्कोनियम (Zr) और टाइटेनियम (Ti) के लिए प्रयुक्त की जाती है।

(vi) वर्णलेखन विधि (Chromatographic Method) यह विधि इस सिद्धान्त पर आधारित है कि अधिशोषक पर मिश्रण के विभिन्न घटकों का अधिशोषण अलग-अलग होता है। सूक्ष्म मात्रा में पाए जाने वाले तत्वों का शुद्धिकरण इस विधि से किया जाता है।
◆ क्षारीय तथा क्षारीय मृदा धातुएँ इनके क्लोराइडों, ऑक्साइडों या हाइड्रॉक्साइडों के विद्युत अपघटन द्वारा प्राप्त की जाती हैं।
◆ सिल्वर के शोधन में बोरेक्स या पोटैशियम नाइट्रेट गालक का कार्य करते हैं।
◆ विद्युत अपघटन के हॉल-हेरॉल्ट प्रक्रम में शुद्ध ऐलुमिना में क्रायोलाइट तथा फ्लोरस्पार मिलाते हैं जिससे ऐलुमिना का गलनांक घट जाता है और इसमें चालकता आ जाती है।
◆ आयरन (III) ऑक्साइड और ऐलुमिनियम का 3 : 1 का मिश्रण थर्मिट मिश्रण कहलाता है और रेल पटरियों को जोड़ने में प्रयुक्त किया जाता है।
◆ पिटवाँ लोहा या आघातवर्ध्य लोहा (wrought or malleable iron) वाणिज्यिक लोहे का शुद्धतम् रूप है।
◆ ढलवाँ लोहा (cast iron), पिटवाँ लोहा और स्टील बनाने में प्रयुक्त होता है।
हमसे जुड़ें, हमें फॉलो करे ..
- Telegram ग्रुप ज्वाइन करे – Click Here
- Facebook पर फॉलो करे – Click Here
- Facebook ग्रुप ज्वाइन करे – Click Here
- Google News ज्वाइन करे – Click Here